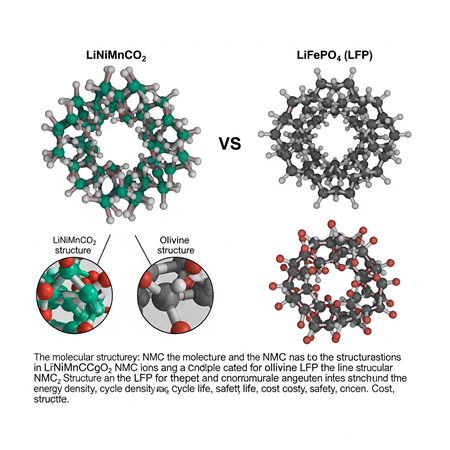
Batarya Teknolojisi: Teknik Derinlemesine NMC ve LFP Batarya Kimyasının Moleküler Farklılıkları
Elektrikli araçların (EV) kalbi olan bataryalar, araçların performansını, menzilini, güvenliğini ve maliyetini doğrudan etkiler. Günümüz piyasasında en yaygın olarak kullanılan iki lityum-iyon batarya kimyası, Nikel Manganez Kobalt (NMC) ve Lityum Demir Fosfat (LFP)'dir. Her iki batarya tipi de lityum iyonlarının hareketine dayanırken, temel farkları katot malzemelerinin moleküler yapısında yatar. Bu farklılıklar, bataryaların karakteristik özelliklerini ve dolayısıyla EV performansını kökten değiştirir.
Bu yazımızda, NMC ve LFP batarya kimyalarının moleküler düzeydeki farklılıklarına inecek, bu yapısal farkların batarya performansına nasıl yansıdığını teknik detaylarıyla açıklayacağız.
Lityum-İyon Bataryaların Temel Çalışma Prensibi
Her lityum-iyon batarya, genel olarak dört ana bileşenden oluşur:
-
Katot (Pozitif Elektrot): Lityum iyonlarının depolandığı ve deşarj sırasında salındığı yer.
-
Anot (Negatif Elektrot): Lityum iyonlarının şarj sırasında depolandığı yer (genellikle grafit).
-
Elektrolit: Lityum iyonlarının katot ile anot arasında hareket etmesini sağlayan iletken ortam.
-
Ayırıcı: Katot ve anotun fiziksel olarak temasını engelleyen, ancak iyon geçişine izin veren gözenekli bir zar.
Şarj ve deşarj döngüsü sırasında, lityum iyonları katot ile anot arasında hareket ederken, elektronlar harici devreden akım oluşturur. Batarya kimyasının temel farkı ise katot malzemesinin moleküler yapısında gizlidir.
NMC (Nikel Manganez Kobalt) Batarya Kimyası: Katmanlı Yapı ve Yüksek Enerji Yoğunluğu
Kimyasal Formül: Genel olarak LiNi?Mn?Co²O² şeklinde ifade edilir. (Burada x+y+z=1 veya yaklaşık 1'dir ve nikel, manganez ve kobaltın oranları değişebilir, örn. NMC 111, NMC 532, NMC 811).
Moleküler Yapı ve İşlevi:
-
Katmanlı Geçiş Metal Oksit Yapısı: NMC bataryaların katodu, lityum iyonlarının geçiş metal oksit katmanları arasında hareket ettiği katmanlı bir yapıya sahiptir. Bu yapı, lityum iyonlarının kolayca yerleşip ayrılabilmesi için geniş alanlar sunar.
-
Nikel (Ni): Katot malzemesinin yüksek enerji yoğunluğundan sorumludur. Nikel, daha fazla lityum iyonunu depolama kapasitesi ve daha yüksek voltaj potansiyeli sunar. Ancak, yüksek nikel içeriği termal kararlılığı azaltabilir.
-
Manganez (Mn): Batarya yapısına termal kararlılık ve güvenlik katmak için kullanılır. Manganez, katot yapısını stabilize ederek aşırı ısınma riskini azaltmaya yardımcı olur ve nikelin reaktivitesini dengeleyebilir.
-
Kobalt (Co): Lityum iyonlarının hareketini kolaylaştırarak iletkenliği artırır ve bataryanın döngü ömrünü uzatmaya yardımcı olur. Ayrıca yapının bütünlüğünü korur. Ancak, kobaltın yüksek maliyeti ve sınırlı arzı, endüstride kobalt içeriğini azaltma eğilimine yol açmıştır (örn. NMC 811 gibi yüksek nikel, düşük kobalt oranları).
Moleküler Avantajları:
-
Yüksek Enerji Yoğunluğu: Katmanlı yapının sunduğu daha geniş depolama alanları ve nikelin yüksek kapasitesi sayesinde, NMC bataryalar birim ağırlık veya hacim başına daha fazla enerji depolayabilir. Bu, araçların daha uzun menzillere ulaşmasını sağlar.
-
Yüksek Güç Çıkışı: Geçiş metallerinin (Ni, Mn, Co) redoks potansiyelleri, yüksek akım çekme ve hızlı ivmelenme için uygun yüksek güç çıkışı sağlar.
-
Düşük Sıcaklık Performansı: Lityum iyonlarının hareketliliği, daha kararlı katmanlı yapı sayesinde düşük sıcaklıklarda LFP'ye göre daha az etkilenir.
Moleküler Dezavantajları:
-
Termal Kararsızlık (LFP'ye Göre): Katmanlı yapı, aşırı ısınma durumlarında termal kaçışa (thermal runaway) daha yatkın olabilir. Kobaltın varlığı, oksijen salınımına ve zincirleme reaksiyonlara daha elverişli bir ortam yaratabilir. Bu yüzden gelişmiş termal yönetim sistemleri zorunludur.
-
Daha Yüksek Maliyet: Özellikle nikel ve kobalt gibi pahalı metallerin kullanımı nedeniyle üretim maliyetleri LFP'ye göre daha yüksektir.
LFP (Lityum Demir Fosfat) Batarya Kimyası: Olivin Yapı ve Yüksek Güvenlik
Kimyasal Formül: LiFePO4
Moleküler Yapı ve İşlevi:
-
Olivin Yapısı: LFP bataryaların katodu, olivin adı verilen son derece kararlı ve sağlam bir kristal yapıya sahiptir. Bu yapı, lityum iyonlarının demir fosfat kafesi içinde hareket ettiği bir "tünel" veya "kanal" sistemi oluşturur.
-
Demir (Fe) ve Fosfat (PO4): Bu elementler, katot yapısının temelini oluşturur. Demir, redoks reaksiyonlarında (Fe²?/Fe³?) rol oynarken, fosfat grubu (PO4) yapının bütünlüğünü ve termal stabilitesini sağlayan güçlü kovalent bağlar oluşturur. Bu güçlü bağlar, bataryanın aşırı ısınma durumlarında bile moleküler yapısını korumasına yardımcı olur.
Moleküler Avantajları:
-
Üstün Termal Kararlılık ve Güvenlik: Olivin yapısındaki demir-fosfat bağları son derece güçlüdür. Bu, bataryanın aşırı şarj, fiziksel hasar veya yüksek sıcaklık gibi stresli koşullar altında bile oksijen salınımına ve termal kaçağa karşı yüksek direnç göstermesini sağlar. Yangın veya patlama riski çok daha düşüktür.
-
Uzun Döngü Ömrü: Güçlü ve kararlı moleküler yapı, şarj/deşarj döngüleri sırasında katot malzemesinin daha az yapısal bozulma yaşamasını sağlar. Bu da LFP bataryalara çok daha uzun bir döngü ömrü kazandırır (binlerce döngüye kadar).
-
Düşük Maliyet: Doğada bol ve ucuz bulunan demir ve fosfat kullanıldığı için kobalt veya nikel gibi pahalı metallere bağımlılık yoktur.
Moleküler Dezavantajları:
-
Daha Düşük Enerji Yoğunluğu: Olivin yapısı, lityum iyonları için NMC'nin katmanlı yapısına göre daha az yer sunar. Ayrıca, demirin daha düşük redoks potansiyeli, NMC'ye kıyasla daha düşük bir voltaj ve dolayısıyla daha düşük bir enerji yoğunluğu anlamına gelir (aynı ağırlık veya hacimde daha az enerji depolama). Bu durum, aynı menzili sağlamak için daha büyük ve ağır bir batarya paketi gerektirebilir. Ancak CTP (Cell-to-Pack) gibi yeni teknolojiler bu dezavantajı azaltıyor.
-
Düşük Sıcaklık Performansı: Düşük sıcaklıklarda lityum iyonlarının olivin kafesindeki hareketliliği azalır, bu da iç direnci artırır ve menzil ile şarj hızında düşüşe neden olabilir.
Moleküler Yapının Performansa Etkisi Özet Tablosu
Sonuç
NMC ve LFP batarya kimyaları arasındaki temel fark, katot malzemelerinin moleküler yapısından kaynaklanır. NMC'nin katmanlı yapısı, yüksek enerji yoğunluğu ve güç çıkışı sağlayarak uzun menzilli ve yüksek performanslı EV'ler için idealdir. Ancak bu, daha yüksek maliyet ve termal yönetim gereksinimi ile gelir. Öte yandan, LFP'nin sağlam olivin yapısı, üstün güvenlik ve çok uzun döngü ömrü sunar ve daha uygun maliyetlidir. Enerji yoğunluğu geleneksel olarak daha düşük olsa da, yeni nesil paketleme teknikleriyle bu fark kapanmaktadır.
Elektrikli araç üreticileri, araçlarının kullanım amacına ve hedef fiyat noktasına göre bu iki batarya kimyasından birini veya ikisinin birleşimini tercih edebilirler. Moleküler düzeydeki bu farklılıkları anlamak, elektrikli araç teknolojisinin temelini kavramak ve gelecek batarya inovasyonlarını takip etmek için kritik öneme sahiptir. Gelecekte, her iki kimyanın da optimize edilmesiyle birlikte, batarya teknolojileri EV'leri daha erişilebilir, daha güvenli ve daha performanslı hale getirmeye devam edecektir.
Bize Ulaşın
-
Kurtköy Mah. Ankara Cad. Yelken Plaza No: 289/21 PENDİK / İSTANBUL
-
+90 216 526 04 90
-
+90 532 134 47 92
-
+90 216 212 01 21
-
+90 532 134 47 92
-
bilgi@nanokar.com.tr
E-Bülten Aboneliği
-
Kampanya ve yeniliklerden haberdar olmak için e-bültenimize kayıt olun.
KURUMSAL
SİPARİŞ

